- Jonathan Dickinson est nommé Président du Directoire
d’Innate Pharma
- Innate a reçu une réponse préliminaire encourageante de la
FDA1 concernant sa stratégie réglementaire pour lacutamab
- Des données relatives à la qualité de vie et à l’analyse
translationnelle de l’étude TELLOMAK avec lacutamab seront
présentées au prochain congrès de l’ASH
- Innate a reçu l’autorisation de la FDA d'initier le
développement clinique d'IPH4502, son conjugué anticorps-médicament
ciblant Nectine-4, dans les tumeurs solides
- Des données précliniques concernant le NK Cell Engager de
nouvelle génération IPH6501 et le conjugué anticorps-médicament
IPH4502 ont été présentées au congrès de la SITC
- Trésorerie, équivalents de trésorerie et actifs financiers
s’élevant à 96,4 millions d’euros2 au 30 septembre 2024, avec un
horizon de trésorerie jusqu’à fin 2025
- Une conférence téléphonique se tiendra aujourd’hui à 14h00
CET
Regulatory News:
Innate Pharma SA (Euronext Paris : IPH ; Nasdaq : IPHA) («
Innate » ou la « Société ») annonce aujourd’hui son
chiffre d’affaires et sa position de trésorerie pour les neuf
premiers mois de l’année 2024.
« J’ai le plaisir de rejoindre Innate Pharma à un moment clé
dans son histoire, » commente Jonathan Dickinson, Président du
Directoire d’Innate Pharma. « Nous avons franchi des étapes
réglementaires notables au cours du trimestre, notamment avec une
réponse préliminaire encourageante de la FDA concernant notre
stratégie réglementaire pour lacutamab et l'autorisation d’initier
le développement clinique d’IPH4502, notre ADC ciblant la
Nectine-4. Grâce aux présentations aux congrès de l'ASH et de la
SITC, qui mettent en évidence la profondeur de notre science
translationnelle et de nos données relatives aux patients, nous
sommes parfaitement positionnés pour faire progresser notre mission
d'apporter de nouvelles solutions thérapeutiques aux patients.
Notre position de trésorerie, qui s'étend jusqu'à la fin de 2025,
nous permet de continuer à aller de l’avant, et j’ai hâte de mener
la Société vers sa prochaine phase de croissance. »
Une conférence téléphonique se
tiendra aujourd’hui à 14h00 CET
Le direct de l'événement sera
disponible au lien suivant :
https://events.q4inc.com/attendee/381945831
Les participants peuvent
également rejoindre la conférence par téléphone en s’inscrivant au
lien ci-après : https://registrations.events/direct/Q4I280043
Ces informations sont également
disponibles dans la rubrique investisseurs du site internet
d’Innate, www.innate-pharma.com. Une rediffusion de la présentation
sera archivée sur le site d'Innate pendant 90 jours après
l'événement.
____________________________
1
Agence américaine du médicament
2
Incluant des investissements court-terme (14,0 millions d’euros) et
des instruments financiers non-courants (10,3 millions d’euros).
Avancées du portefeuille :
Lacutamab (anticorps anti-KIR3DL2)
:
Lymphomes T cutanés
TELLOMAK est un essai clinique de Phase 2, ouvert et
multicohorte, évaluant lacutamab chez des patients atteints d’un
syndrome de Sézary ou d’un mycosis fongoïde.
- Au cours du troisième trimestre 2024, Innate a reçu une réponse
préliminaire encourageante de la FDA concernant sa stratégie
réglementaire pour lacutamab, y compris une potentielle
autorisation accélérée dans le syndrome de Sézary. La Société
continuera d’échanger avec la FDA en ce qui concerne un essai
confirmatoire de Phase 3.
- Les résultats de l’étude dans le syndrome de Sézary et le
mycosis fongoïde ont été présentés au congrès de l’association
américaine d’hématologie (American Society of Hematology - ASH)
2023 et au congrès de la société américaine d’oncologie clinique
(American Society of Clinical Oncology - ASCO) 2024
respectivement.
- Les données portant sur la qualité de vie et l’analyse
translationnelle de l’étude TELLOMAK chez les patients présentant
un lymphome T cutané en rechute et/ou réfractaire seront présentées
au congrès de l’ASH 2024.
Lymphomes T périphériques
L'essai de Phase 2 KILT (anti-KIR in T Cell Lymphoma), un essai
contrôlé randomisé mené par la Lymphoma Study Association (LYSA),
évalue lacutamab en combinaison avec le régime de chimiothérapie
GEMOX (gemcitabine en combinaison avec oxaliplatine) contre GEMOX
seul chez des patients atteints de lymphomes T périphériques en
rechute ou réfractaires exprimant KIR3DL2, est en cours et continue
de recruter des patients.
ANKET®
(Antibody-based NK cell
Engager Therapeutics)
:
ANKET® est la plateforme propriétaire d’Innate permettant de
développer une nouvelle génération de NK cell engagers
multi-spécifiques pour traiter certains types de cancer. Cinq
candidats-médicaments sont à ce jour issus de la plateforme ANKET®
: SAR443579/IPH6101 (SAR’579 ; NK Cell Engager trifonctionnel
anti-CD123), SAR445514/IPH6401 (SAR’514 ; NK Cell Engager
trifonctionnel anti-BCMA), IPH62 (anti-B7-H3), IPH67 (cible non
divulguée, tumeurs solides) et le tétra-spécifique IPH6501
(anti-CD20 comprenant un IL-2v). D’autres cibles précliniques
propriétaires non divulguées sont en cours d’investigation.
IPH6501 (propriétaire)
IPH6501 est le produit ANKET® de seconde génération propriétaire
d'Innate comprenant un IL-2v et ciblant le CD20. L'essai clinique
de Phase 1/2 évaluant IPH6501 dans le lymphome non hodgkinien à
cellules B est en cours et continue de recruter des patients.
- Des données précliniques soutenant l’évaluation d’IPH6501 dans
les sous-types de lymphomes non-hodgkiniens à cellules B en rechute
ou réfractaire et après un traitement à base de CAR-T ont été
présentées au congrès de la société pour l’immunothérapie des
cancer (Society for Immunotherapy of Cancer - SITC) 2024.
SAR’579/IPH6101, SAR’514/IPH6401, IPH62 et IPH67 (en
partenariat avec Sanofi)
SAR’579/IPH6101
L’essai clinique de Phase 1/2 mené par Sanofi évaluant SAR’579 /
IPH6101 chez des patients atteints de leucémie aiguë myéloïde
récidivante ou réfractaire, de leucémie aiguë lymphoblastique à
cellules B ou d’un syndrome myélodysplasique de haut risque
progresse de manière satisfaisante. SAR’579 / IPH6101 est le
premier NK cell engager co-engageant NKp46, CD16 et ciblant CD123,
issu de la plateforme ANKET®.
SAR’514/IPH6401
L’essai clinique de Phase 1/2 mené par Sanofi évaluant SAR’514 /
IPH6401, un NK cell engager co-engageant NKp46, CD16 et ciblant
BCMA, chez des patients présentant un myélome multiple en
rechute/réfractaire et une amylose AL en rechute/réfractaire est en
cours.
IPH62, IPH67 et option
- IPH62 est un programme de NK Cell Engager issu de la plateforme
ANKET® ciblant B7-H3 en cours de développement. Suite à une période
de collaboration de recherche et suite à la sélection du
candidat-médicament, Sanofi sera responsable du développement, de
la fabrication et de la commercialisation des produits.
- Au cours du troisième trimestre 2024, Sanofi a mis fin à la
licence concernant IPH67 au cours de la période de collaboration de
recherche. Par conséquence, Innate prévoit de récupérer
l’intégralité des droits sur IPH67, un programme de NK Cell Engager
issu de la plateforme ANKET® en cours de développement dans les
tumeurs solides. Le reste de l’accord de collaboration et de
licence de 2022 avec Sanofi est inchangé.
- Sanofi conserve une option de licence pour une cible
additionnelle ANKET® conformément à l’accord de collaboration et de
licence de 2022.
Conjugués Anticorps-Médicaments (ADC)
:
Innate met à profit son expertise en ingénierie des anticorps
pour développer des formats de conjugués anticorps-médicaments
(antibody drug conjugates - ADC).
IPH4502 (ADC anti-Nectine-4) :
IPH4502 est un ADC ciblant Nectine-4 et différencié à base
d’exatecan, un inhibiteur de topoisomérase I, comme agent
cytotoxique.
- En septembre 2024, Innate a reçu l'autorisation de l'agence
américaine du médicament d'initier le développement clinique
d'IPH4502 avec un essai clinique de Phase 1 dans les tumeurs
solides connues pour exprimer la Nectine-4. Innate souhaite initier
l’essai de Phase 1 au premier trimestre 2025 au plus tard.
- L'étude de Phase 1, ouverte et multicentrique, comprendra une
partie 1 d’escalade de la dose et une partie 2 d'optimisation de la
dose et évaluera la sécurité, la tolérance et l'efficacité
préliminaire d’IPH4502 en monothérapie dans les tumeurs solides
avancées connues pour exprimer Nectine-4, comme le carcinome
urothélial, les cancers du poumon non à petites cellules, du sein,
de l’ovaire, gastrique ou colorectal.
- Des données précliniques soutenant le développement d’IPH4502
dans les tumeurs connues pour exprimer la Nectine-4 ont été
présentées au congrès du SITC 2024.
Monalizumab (anticorps anti-NKG2A), en
partenariat avec AstraZeneca :
- L’étude de Phase 3 PACIFIC-9 menée par AstraZeneca évaluant
durvalumab (anti-PD-L1) en combinaison avec monalizumab
(anti-NKG2A) ou oleclumab (l’anti-CD73 d’AstraZeneca) chez des
patients atteints d’un cancer du poumon non à petites cellules, de
stade III, non opérable, qui n'ont pas progressé après une
chimio-radiothérapie simultanée à base de sels de platine, est en
cours. Un comité indépendant de contrôle des données a recommandé
la poursuite de l’essai de Phase 3 PACIFIC-9 sur la base une
analyse intermédiaire prévue au protocole.
IPH5201 (anti-CD39), en partenariat
avec AstraZeneca :
- L’essai clinique de Phase 2 MATISSE, mené par Innate, dans le
cancer du poumon avec un traitement pré-opératoire incluant
IPH5201, un anticorps monoclonal anti-CD39 développé en partenariat
avec AstraZeneca est en cours et le recrutement des patients se
poursuit. A la suite d’une analyse intérimaire planifiée, l’essai
clinique de Phase 2 MATISSE se poursuit conformément aux
plans.
IPH5301 (anti-CD73) :
- L’essai clinique de Phase 1 avec IPH5301 (CHANCES) en
collaboration avec l’Institut Paoli-Calmettes est en cours.
Annonce Corporate
- Le Conseil de Surveillance d’Innate a nommé Jonathan Dickinson
au poste de Président du Directoire. La nomination a pris effet le
1er novembre 2024. Jonathan Dickinson succède à Hervé Brailly,
co-fondateur de la Société et Président du Directoire par intérim
durant la période de recherche. Jonathan Dickinson occupait le
poste de Vice-Président Exécutif et Directeur Général Europe chez
Incyte depuis 2016. Avant de rejoindre Incyte, Jonathan Dickinson a
eu des responsabilités de cadre dirigeant à fort leadership chez
ARIAD Pharmaceuticals, une biotech américaine spécialisée en
oncologie, et chez Bristol-Myers Squibb. Il a auparavant passé 13
ans chez Hoffmann-La Roche, où il a contribué au succès de
plusieurs produits phares en oncologie. Jonathan Dickinson a
commencé sa carrière chez Novartis, où il a occupé des postes à
responsabilité croissante dans les divisions d'oncologie et
d'endocrinologie. Il est titulaire d'une licence en génétique et
d'un master en administration des affaires de l'université de
Nottingham (Royaume-Uni).
- Le programme At-The-Market (ATM) selon lequel la Société peut
émettre auprès d’investisseurs éligibles un montant brut total
allant jusqu'à 75 millions de dollars d'American Depositary Shares
(« ADS ») est en cours. Au 30 juin 2024, aucune vente n’a été
réalisée dans le cadre de ce programme.
Résultats financiers au troisième trimestre 2024 :
Au 30 septembre 2024, la trésorerie, les équivalents de
trésorerie et actifs financiers de la Société s’élevaient à 96,4
millions d’euros. À la même date, le total des passifs financiers
de la Société s’élevait à 33,2 millions d’euros.
Le chiffre d’affaires pour les neuf premiers mois de 2024
s’élevait à 10,2 millions d’euros comparé à 36,5 millions d’euros
pour les neuf premiers mois de 2023. Pour la période de neuf mois
se terminant le 30 septembre 2024, le chiffre d’affaires provient
majoritairement de la reconnaissance partielle ou intégrale des
paiements reçus dans le cadre des accords de collaboration et de
licence avec AstraZeneca et Sanofi.
A propos d’Innate Pharma
Innate Pharma S.A. est une société de biotechnologies au stade
clinique qui développe des traitements d’immunothérapies contre le
cancer. Son approche innovante vise à tirer avantage du système
immunitaire inné par le biais de trois approches thérapeutiques :
les anticorps monoclonaux, les NK Cell Engagers issus de sa
plateforme propriétaire ANKET® (Antibody-based NK
cell Engager Therapeutics) et les conjugués
anticorps-médicaments.
Le portefeuille d'Innate comprend notamment le programme
propriétaire lacutamab, développé dans des formes avancées de
lymphomes T cutanés T et de lymphomes T périphériques, monalizumab
développé avec AstraZeneca dans le cancer du poumon non à petites
cellules, ainsi que des NK Cell Engagers multi-spécifiques issus de
sa plateforme ANKET® et pouvant cibler différents types de cancers
ainsi qu’IPH4502, un conjugué anticorps-médicament différencié en
développement dans les tumeurs solides.
Afin d'accélérer l'innovation, la recherche et le développement
de traitements au bénéfice des patients, Innate Pharma est un
partenaire de confiance pour des sociétés biopharmaceutiques
leaders telles que Sanofi et AstraZeneca, ainsi que pour les
institutions de recherche de premier plan.
Basée à Marseille, avec une filiale à Rockville (Maryland,
Etats-Unis), Innate Pharma est cotée en bourse sur Euronext Paris
et sur le Nasdaq aux Etats-Unis.
Retrouvez Innate Pharma sur www.innate-pharma.com et suivez nos
actualités sur LinkedIn et sur X.
Informations pratiques :
Code ISIN
Code mnémonique
LEI
FR0010331421
Euronext : IPH Nasdaq : IPHA
9695002Y8420ZB8HJE29
Avertissement concernant les informations prospectives et les
facteurs de risques :
Ce communiqué de presse contient des déclarations prospectives,
y compris celles visées par les lois sur les valeurs mobilières
applicables, notamment le Private Securities Litigation Reform Act
de 1995. L'emploi de certains termes, notamment « anticiper », «
croire », « potentiel », « estimer », « s'attendre à » et « sera »
et leur contraire ainsi que d'autres expressions semblables, vise à
identifier des énoncés prospectifs. Bien que la Société considère
que ses projections sont basées sur des hypothèses raisonnables,
ces déclarations prospectives peuvent être remises en cause par un
certain nombre d’aléas et d’incertitudes, ce qui pourrait donner
lieu à des résultats substantiellement différents de ceux
anticipés. Ces aléas et incertitudes comprennent notamment les
incertitudes inhérentes à la recherche et développement, y compris
celles relatives à l’innocuité, aux progrès et aux résultats des
essais cliniques et des études précliniques en cours ou prévus, aux
examens et autorisations d’autorités réglementaires concernant les
produits-candidats de la Société, la dépendance de la Société à
l'égard de tiers pour la fabrication de ses produits candidats, des
efforts commerciaux de la Société, la capacité de la Société à
continuer à lever des fonds pour son développement. Pour des
considérations supplémentaires en matière de risques et
d’incertitudes pouvant faire différer les résultats effectifs, la
situation financière, la performance et les réussites de la
Société, merci de vous référer à la section « Facteurs de Risques »
du Document d’Enregistrement Universel déposé auprès de l’Autorité
des marchés financiers (AMF), disponible sur les sites Internet
d’Innate Pharma (www.innate-pharma.com) et de l’AMF
(www.amf-france.org), et les documents et rapports publics déposés
auprès de la Securities and Exchange Commission (SEC) des
États-Unis, y compris le rapport annuel sur « Form 20-F » pour
l’exercice clos le 31 décembre 2023 et les documents et rapports
subséquents déposés auprès de l'AMF ou de la SEC, ou autrement
rendus publics, par la Société. Les références au site internet de
la Société et au site internet de l'AMF sont incluses à titre
d'information uniquement et le contenu de ces sites, ou auquel il
est possible d'accéder par leur intermédiaire, n'est pas incorporé
par référence dans le présent communiqué de presse et n'en
constitue pas une partie intégrante.
Compte tenu des incertitudes significatives liées à ces
déclarations prospectives, vous ne devez pas considérer ces
déclarations comme une déclaration ou une garantie de la part de la
Société ou de toute autre personne que la Société atteindra ses
objectifs et ses plans dans un délai donné ou même qu'elle les
atteindra. La Société ne s'engage pas à mettre à jour publiquement
les déclarations prospectives, que ce soit à la suite de nouvelles
informations, d'événements futurs ou autres, sauf si la loi
l'exige.
Le présent communiqué, et les informations qu’il contient, ne
constituent ni une offre de vente ou de souscription, ni la
sollicitation d’un ordre d’achat ou de souscription, des actions
d’Innate Pharma dans un quelconque pays.
Consultez la
version source sur businesswire.com : https://www.businesswire.com/news/home/20241112568209/fr/
Pour tout renseignement complémentaire, merci de contacter
: Relation investisseurs
Innate Pharma Henry Wheeler Tel.: +33 (0)4 84 90 32 88
Henry.wheeler@innate-pharma.fr Médias NewCap Arthur Rouillé Tel.: +33
(0)1 44 71 00 15 innate@newcap.eu
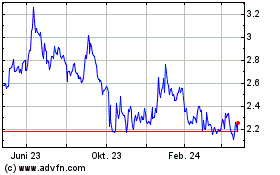
Innate Pharma (EU:IPH)
Historical Stock Chart
Von Okt 2024 bis Nov 2024
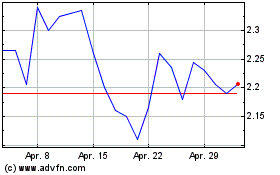
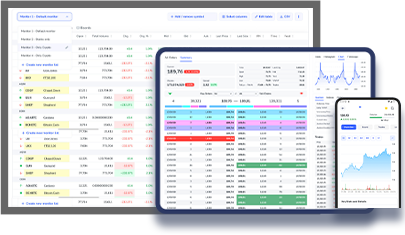
Innate Pharma (EU:IPH)
Historical Stock Chart
Von Nov 2023 bis Nov 2024